УДК 543.42; 543.062
СИНТЕЗ ПЕНОПОЛИУРЕТАНА, МОДИФИЦИРОВАННОГО НАНОЧАСТИЦАМИ ЗОЛОТА, И ЕГО ИСПОЛЬЗОВАНИЕ ДЛЯ ОПРЕДЕЛЕНИЯ АСКОРБИНОВОЙ КИСЛОТЫ
© 2010 г. М.Н. Марагаева, П.А. Волков, В.В. Архипова, В.В. Апяри
Московский
государственный университет имени М.В. Ломоносова,
химический факультет
119991 Москва, ГСП-2, Ленинские горы, 1, стр.3
Изучена возможность синтеза пенополиуретана, модифицированного наночастицами золота путем сорбции золотохлористоводородной кислоты и ее последующего восстановления в фазе пенополиуретана аскорбиновой кислотой. Изучено влияние различных факторов на сорбцию золотохлористоводородной кислоты и ее восстановление в пенополиуретане. Модифицированный наночастицами золота пенополиуретан использован в роли аналитической формы в спектроскопии диффузного отражения для определения аскорбиновой кислоты с пределом обнаружения 0,05 мкг/мл. Диапазон линейности составил 0,15 – 1 мкг/мл. Способ применен для определения аскорбиновой кислоты в витамине «Ревит».
Ключевые слова: пенополиуретан, наночастицы золота, спектроскопия диффузного отражения, определение аскорбиновой кислоты
Наночастицы, то есть частицы с размерами от единиц до сотен нанометров, привлекают в последнее время большое внимание в различных областях химии, физики, медицине и фотонике [1]. Среди наночастиц и наноструктур, особое место занимают наночастицы (НЧ) золота, которые благодаря своим уникальным физическим и химическим свойствам и относительной простоте получения широко используют в биохимии и медицине, иммунохимии, катализе, химическом анализе и других отраслях науки [2 – 4].
Направления использования наночастиц золота в химическом анализе разнообразны. Их применяют в электрохимическом и биоэлектрохимическом анализе [5, 6], в хроматографических и электрофоретических методах [7, 8], для усиления сигнала пьезокварцевых сенсоров, в химических и иммуносенсорах [9 – 11]. Кроме того, в последние 10 лет появились работы, указывающие на то, что НЧ золота можно использовать в качестве спектрофотометрических реагентов и в спектрофотометрии и тест-методах анализа.
Стратегия применения наночастиц золота в спектрофотометрическом анализе в большинстве случаев сводится к следующему: к раствору определяемого компонента добавляют определенное количество предварительно синтезированных НЧ золота и регистрируют изменения оптических характеристик анализируемых растворов спектрофотометрически или визуально. В биохимии наночастицы золота часто используются в индикаторных тест-полосках. Основными их преимуществами являются стабильность, легкость визуального детектирования и экспрессность аналитической процедуры.
Уникальные оптические свойства наночастиц золота обусловлены явлением поверхностного плазмонного резонанса (ППР), которое проявляется в возникновении интенсивной полосы поглощения в видимой области спектра и резкой зависимости ее положения от степени агрегации наночастиц [12 – 14]. Этот эффект используют для разработки спектрофотометрических методик определения ионов металлов, анионов и органических соединений, каким-либо образом изменяющим интенсивность полосы ППР или приводящим к ее смещению. К недостаткам описанного подхода можно отнести зачастую узкий диапазон линейности градуировочных зависимостей, малое изменение оптической плотности, невозможность работы в мутных и окрашенных средах. Проблему можно было бы решить в рамках сорбционно-спектроскопических методов анализа. В настоящей работы для этой цели предложено использовать пенополиуретан. Этот полимерный материал обладает рядом существенных достоинств, необходимых для разработки сорбционно-спектроскопических методов, таких как отсутствие собственной окраски, химическая устойчивость, механическая прочность в сочетании с эластичностью, легкость отделения от раствора, дешевизна и доступность.
Цель настоящей работы состояла в изучении возможности синтеза пенополиуретана, модифицированного наночастицами золота, и использования его в роли аналитической формы для определения аскорбиновой кислоты с помощью спектроскопии диффузного отражения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты, аппаратура и техника эксперимента. В качестве сорбента применяли пенополиуретан (ППУ) 5-30 на основе простых полиэфиров. Сорбент использовали в виде таблеток (высота 5 мм, диаметр – 16 мм, масса ~0,02 г), которые выбивали металлическим пробойником из промышленного листа полимера. Для очистки от примесей таблетки ППУ встряхивали с ацетоном, после чего высушивали до воздушно-сухого состояния. Таблетки хранили в защищенном от света месте.
В работе использовали золотохлористоводородную кислоту (х.ч.), аскорбиновую кислоту (ч.д.а.), серную кислоту (х.ч.), гидроксид натрия (ч.). Исходные водные растворы золотохлористоводородной и аскорбиновой кислот готовили растворением их точных навесок в дистиллированной воде.
Спектры диффузного отражения в видимой области и диффузное отражение регистрировали с помощью мини-спектрофотометра-калибратора мониторов Eye-One Pro (GretagMacbeth, Швейцария)
О содержании наночастиц золота в фазе ППУ судили, измеряя значения функции Кубелки-Мунка F при длине волны, соответствующей максимуму поглощения (lmax):
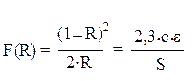
где R — диффузное отражение; e — молярный коэффициент поглощения сорбата, М-1 см-1; c — его концентрация, М; S — коэффициент рассеивания, см-1.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В настоящей работе изучена возможность получения композитного материала на основе ППУ и наночастиц золота. Предложен способ получения такого материала. Способ основан на сорбции золота в виде HAuCl4 пенополиуретаном из водного раствора и последующем восстановлении тетрахлораурат-ионов непосредственно в фазе ППУ. В качестве восстановителя использовали аскорбиновую кислоту, выбор которой в этом качестве был обусловлен актуальностью поиска подходов к ее определению, а также как модельное соединение – представителя класса органических соединений-восстановителей.
Важным с точки зрения аналитической химии является то, что в фазе ППУ наночастицы золота сохраняют способность к поверхностному плазмонному резонансу (ППР), который проявляется в поглощении светового излучения в области 520 – 540 нм. Образцы ППУ, содержащего наночастицы золота, окрашены в красно-фиолетовый цвет и могут быть использованы в качестве удобной аналитической формы в спектроскопии диффузного отражения и тест-методах при определении восстановителей. Поэтому изучение особенностей образования наночастиц золота в матрице ППУ и влияния на него различных факторов представляет интерес.
Сорбция золотохлористоводородной кислоты пенополиуретаном. Сорбцию HAuCl4 на ППУ проводили в статическом режиме. Для этого таблетки ППУ помещали в 5 мл раствора HAuCl4, прожимали их стеклянной палочкой для удаления пузырьков воздуха из пор и встряхивали на механическом шейкере в течение 40 мин. Таблетки вынимали, высушивали фильтровальной бумагой и измеряли диффузное отражение.
Установлено, что из водных растворов HAuCl4 сорбируется на ППУ на 98 – 100%, при этом таблетки ППУ приобретают интенсивно желтый цвет. В спектрах диффузного отражения сорбатов (рис. 1а) наблюдается полоса с максимумом при 400 – 410 нм, значение функции Кубелки-Мунка в максимуме увеличивается с ростом концентрации HAuCl4 в водном растворе. Уширение спектров по мере увеличения содержания HAuCl4 в матрице ППУ вероятно обусловлено взаимодействием HAuCl4 с матрицей пенополиуретана. На рис. 1б представлена зависимость F410 от концентрации исходного раствора HAuCl4. Из рисунка можно сделать вывод о том, что функция Кубелки-Мунка линейно зависит от концентрации исходного раствора до 50 – 60 мкг/мл по золоту, после чего достигается предельная сорбция. Таким образом, предельная сорбция HAuCl4 на ППУ составляет 310 мкг/табл. ППУ в пересчете на золото, или 15,5 мг/г сорбента (79 мкмоль/г сорбента).
Сорбция HAuCl4 не зависит от кислотности раствора в интервале рН 1 – 4,5; при дальнейшем увеличении рН сорбция уменьшается.
Влияние различных факторов на формирование наночастиц золота в матрице пенополиуретана. Для изучения возможности синтеза НЧ в полимере таблетки ППУ, модифицированного HAuCl4, помещали в раствор аскорбиновой кислоты, встряхивали на механическом шейкере в течение определенного времени, вынимали, просушивали между листами фильтровальной бумаги и измеряли спектры диффузного отражения. Было установлено, что пенополиуретан, модифицированный HAuCl4, реагирует с водными растворами аскорбиновой кислоты с образованием в его фазе наночастиц золота. Это сопровождается изменением окраски сорбента и появлением в спектре диффузного отражения полосы при 540 нм.
Изучено влияние различных факторов на восстановление HAuCl4 в фазе ППУ: содержания HAuCl4 в фазе сорбента, кислотности среды, присутствия катионного ПАВ (ЦТМА), а также концентрации аскорбиновой кислоты. Рассмотрим влияние этих факторов последовательно.
Влияние содержания HAuCl4. В работе изучено влияние содержания HAuCl4 в ППУ на выход наночастиц в твердой фазе при восстановлении аскорбиновой кислотой.
Таблетки ППУ, содержащие 3,75; 7,5 и 15 мг (Au)/г сорбента вносили в 10 мл раствора аскорбиновой кислоты с концентрацией 20 мкг/мл. Спектры диффузного отражения регистрировали 2 раза – до реакции с аскорбиновой кислотой и после. Зависимость изменения функции Кубелки-Мунка при 540 нм от содержания золота в матрице ППУ приведена на рис. 2. Из представленных данных видно, что сигнал, связанный с формированием наночастиц в ППУ максимален при содержании золота в ППУ 7,5 – 15 мг/г, что соответствует концентрации золота в растворе для модифицирования 30 – 60 мкг/мл.
Влияние кислотности. Изучено влияние кислотности раствора на образование наночастиц золота в фазе ППУ. Восстановление проводили в 0,1 М H2SO4, при рН 5 и в 0,1 М NaOH. Результаты в виде гистограммы представлены на рис. 3, из которого видно, что кислотность среды практически не сказывается на процессе восстановления HAuCl4 аскорбиновой кислотой. Во всех дальнейших экспериментах восстановление проводили при рН 5.
Влияние ЦТМА. На примере бромида цетилтриметиламмония (ЦТМА) изучено влияние КПАВ на процесс восстановления золота до наночастиц в фазе ППУ. Восстановление проводили в присутствии добавки бромида цетилтриметиламмония, которую вводили в раствор аскорбиновой кислоты, и без нее.
Из сравнения спектров диффузного отражения, представленных на рис. 4 видно, что в отсутствие ЦТМА в фазе ППУ образуются агрегаты наночастиц, в спектре наблюдается широкая полоса в области 600 – 700 нм. В присутствии ЦТМА процесс восстановления протекает с образованием индивидуальных наночастиц, в спектре возникает полоса при 540 нм. По аналогии с литературными данными можно предположить, что ЦТМА выступает в качестве стабилизатора наночастиц. Кроме того, наличие в водном растворе катиона ПАВ облегчает транспорт аскорбиновой кислоты через межфазную границу вода – ППУ.
Изучено влияние концентрации ЦТМА на выход наночастиц в ППУ. Зависимость F при 540 нм от концентрации ЦТМА приведена на рис. 5. Из рисунка видно, что значение функции Кубелки-Мунка при 540 нм возрастает при увеличении концентрации ЦТМА до 10 мкг/мл, после чего зависимость выходит на плато. В дальнейших исследованиях использовали концентрацию ЦТМА 20 мкг/мл.
Влияние концентрации аскорбиновой кислоты на выход наночастиц золота в фазе ППУ изучено в интервале 0 – 20 мкг/мл. Восстановление проводили с добавкой ЦТМА (20 мкг/мл) в течение 30 мин. Установлено, что зависимость функции Кубелки-Мунка при 540 нм от концентрации аскорбиновой кислоты линейна до 2 мкг/мл (рис. 6).
Аналитическое использование процессов формирования наночастиц золота в матрице пенополиуретана для определения аскорбиновой кислоты. Функция Кубелки-Мунка в максимуме полосы ППР наночастиц золота в матрице пенополиуретана линейно связана с концентрацией аскорбиновой кислоты в водном растворе, что указывает на принципиальную возможность использования процессов их формирования для определения аскорбиновой кислоты с применением спектроскопии диффузного отражения.
Для построения градуировочного графика в сосуды с притертыми пробками вводили от 0 до 10 мкг аскорбиновой кислоты, добавляли по 200 мкг ЦТМА и воду до общего объема 10 мл. В растворы помещали таблетки ППУ, предварительно модифицированного HAuCl4 из 5 мл раствора с концентрацией золота 30 мкг/мл. Таблетки прожимали стеклянной палочкой для удаления пузырьков воздуха и встряхивали на механическом шейкере в течение 30 мин. Образцы вынимали, высушивали фильтровальной бумагой и измеряли их диффузное отражение при 540 нм. Градуировочный график строили в координатах F540 – c, где с – концентрация аскорбиновой кислоты в растворе.
Градуировочная зависимость линейна в интервале концентраций аскорбиновой кислоты 0,15 – 1,0 мкг/мл. Предел обнаружения, рассчитанный по 3S-критерию, составляет 0,05 мкг/мл. Правильность методики подтверждена методом «введено-найдено» при анализе модельного раствора, приготовленного на дистиллированной воде. При определении 0,50 мкг/мл аскорбиновой кислоты найдено 0,53 ± 0,05 мкг/мл (sr=0,04, n = 3, Р = 0,95).
Проведено определение аскорбиновой кислоты в образце витамина «Ревит», содержащего по данным производителя 35 мг аскорбиновой кислоты на 1 драже. Кроме аскорбиновой кислоты препарат содержал ретинола пальмитат (1,38 мг), тиамина гидрохлорид (1 мг), рибофлавин (1 мг) и сахарозу.
Для проведения определения одно драже препарата измельчали в ступке и растворяли в небольшом количестве воды. Не растворившиеся в воде компоненты отфильтровывали, а растворы доводили водой до 100 мл. Аликвоту 1 мл полученного раствора переносили в мерную колбу на 50 мл и доводили водой до метки. Далее поступали, как описано выше при построении градуировочного графика, вводя в сосуды по 1 мл полученного раствора. Рассчитанное на основании экспериментальных данных содержание аскорбиновой кислоты в препарате составляет 36 ± 6 мг, что хорошо согласуется с данными, заявленными производителем. Относительное стандартное отклонение не превышает 0,06.
Таким образом, осуществлен синтез наночастиц золота непосредственно в матрице пенополиуретана путем восстановления сорбированной на ППУ золотохлористоводородной кислоты аскорбиновой кислотой. Изучено влияние на выход наночастиц кислотности раствора, времени контакта фаз, концентрации аскорбиновой кислоты и бромида цетилтриметиламмония. Показано, что функция Кубелки-Мунка в максимуме полосы ППР наночастиц в матрице ППУ линейно связана с концентрацией аскорбиновой кислоты в растворе, что может быть использовано для ее определения с помощью спектроскопии диффузного отражения с пределом обнаружения 0,05 мкг/мл. Проведено определение аскорбиновой кислоты в витаминном препарате «Ревит».
Рис. 1. Спектры диффузного отражения ППУ, модифицированного HAuCl4, в зависимости от ее концентрации в растворе (а) и зависимость функции Кубелки-Мунка при 410 нм образцов ППУ, модифицированных HAuCl4, от концентрации золота в растворе (б).
V = 5 мл, t = 40 мин. а)аAu мкг/мл: 15 (1), 30 (2), 60 (3), 100 (4).
Рис. 2. Спектры диффузного отражения ППУ, модифицированного HAuCl4, до реакции с аскорбиновой кислотой (1) и после нее (2).
сAu = 15 мг/г, саск. = 20 мкг/мл, с(H2SO4) = 0,05 М, V = 10 мл, t = 30 мин.
Рис. 3. Зависимость изменения функции Кубелки-Мунка при 540 нм от содержания золота в матрице ППУ.
сАК = 20 мкг/мл, с(H2SO4) = 0,05 М, V = 10 мл, t = 30 мин.
Рис. 4. Значения функции Кубелки-Мунка при 540 нм, для образцов ППУ – НЧ золота, полученных восстановлением аскорбиновой кислотой, в зависимости от кислотности среды.
аAu = 7,5 мг/г, саск. = 20 мкг/мл, V = 10 мл, t = 30 мин.
Рис. 5. Спектры диффузного отражения ППУ, модифицированного наночастицами золота, в отсутствие (1) и в присутствии ЦТМА (2).
аAu=7,5 мг/г, сАК=20 мкг/мл, сЦТМА=10 мкг/мл, V=10 мл, t=30 мин.
Рис. 6. Зависимость функции Кубелки-Мунка при 540 нм для ППУ, модифицированного наночастицами серебра, от концентрации ЦТМА.
аAu = 7,5 мг/г, сАК = 20 мкг/мл, V = 10 мл, t = 30 мин.
Рис. 7. Зависимость функции Кубелки-Мунка при 540 нм для образцов ППУ, модифицированного наночастицами золота, от концентрации аскорбиновой кислоты.
аAu = 7,5 мг/г, сЦТМА = 20 мкг/мл, V = 10 мл, t = 30 мин
а б
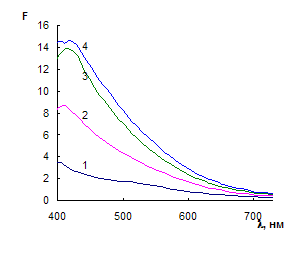
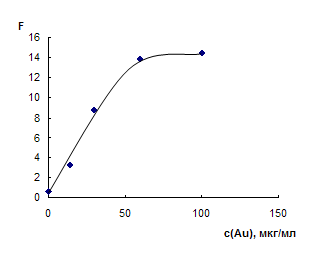 Рис. 1.
Рис. 1.
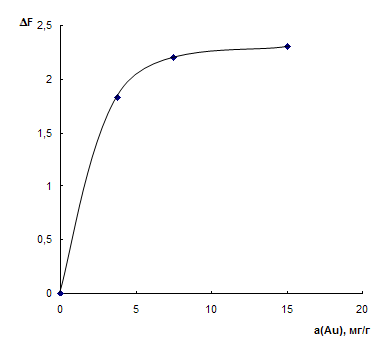 Рис. 2.
Рис. 2.
F540
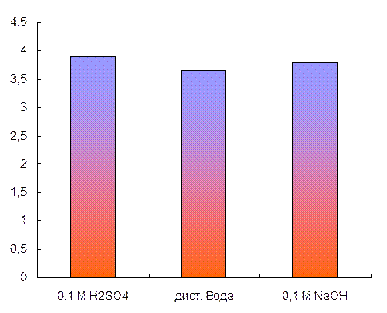 Рис. 3.
Рис. 3.
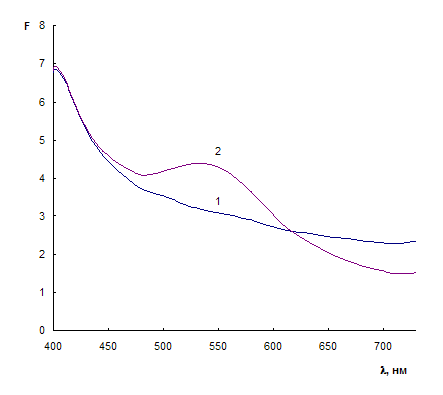 Рис. 4.
Рис. 4.
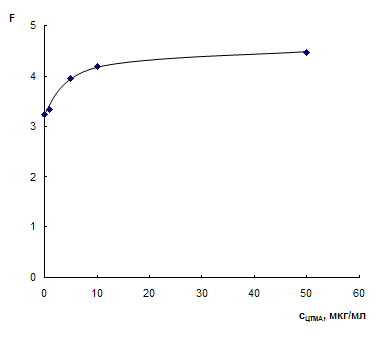 Рис. 5.
Рис. 5.
сАК, мкг/мл ∆F
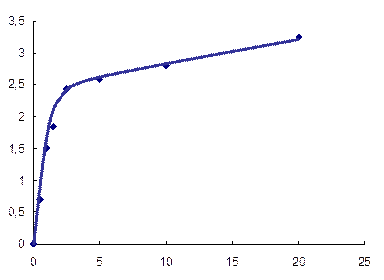
 Рис. 6.
Рис. 6.
СПИСОК ЛИТЕРАТУРЫ